Abstract
Objective: To investigate myocardial tissue alterations in patients with MINOCA using magnetic resonance imaging. Materials and methods: The study included 94 patients with NSTEMI and <50% coronary stenosis. The mean patient age was 62.35±10.33 years (range 33–86), with 78.7% men and 21.3% women. All patients underwent ECG, echocardiography, coronary angiography, and cardiac magnetic resonance imaging with late gadolinium enhancement. Segmental analysis was performed, and quantitative assessment of infarct and edema volumes was conducted. The myocardial perfusion territory was divided into regions supplied by the left anterior descending artery, left circumflex artery, and right coronary artery. Infarct and edema sizes were calculated using Circle Cardiovascular Imaging 42, version 5.1. The infarct area was defined as hyperenhanced myocardium on late gadolinium enhancement images. Results: ECG findings revealed ST-segment depression in 60.6%, T-wave inversion in 48.9%, and conduction disturbances in 11.7% of patients. Clinical condition was satisfactory in 81.9% of patients, while 18.1% had signs of left ventricular failure (Killip class II). The mean GRACE score was 130±20 points. Global longitudinal strain, global longitudinal strain rate, and global circumferential strain were reduced in the MINOCA group compared with the control group (P < 0.05). Mild or moderate stenosis was identified in 52.1% of patients. A total of 1508 myocardial segments were analyzed; among them, 390 exhibited edema and 255 showed infarction. Edema and infarction were most frequently located in the perfusion territory of the left anterior descending artery. Most infarctions were of low transmural extent. Conclusion: Cardiac magnetic resonance imaging is an indispensable tool for assessing the morphological and functional characteristics of the myocardium in patients with MINOCA. MRI not only refines the diagnosis but also enhances risk stratification, improves disease course prediction, and assists in selecting optimal treatment strategies. The use of MRI in clinical practice contributes to a deeper understanding of myocardial injury mechanisms and improves the quality of care for this patient population.
Full article
Инфаркт миокарда без подъема сегмента ST (ИМбпST) с необструктивными коронарными артериями (MINOCA) — это клинический синдром, при котором у пациентов обнаруживается повреждение миокарда, несмотря на отсутствие гемодинамически значимого стеноза коронарных артерий (стеноз <50%) при ангиографии [1]. Это гетерогенное состояние включает разнообразные патофизиологические механизмы, приводящие к ишемии миокарда и некрозу без значительной коронарной обструкции. МINОCА (myocardial infarction with nonobstructive coronaryeries) можно разделить на случаи с отсутствием или минимальным атеросклерозом (стеноз 0–30%) и случаи с умеренным атеросклерозом (стеноз 30–49%) [2].
По данным различных исследований MINOCA встречается у 5–15% пациентов с ИМбпST и является клинической проблемой из-за неоднородной этиологии [3]. В связи с разнообразием этиологии МINOCA следует рассматривать с оперативной диагностикой, требующей системного подхода для определения основной этиологии. Диагноз MINOCA устанавливается, когда пациенты соответствуют критериям острого инфаркта миокарда (ИМ), как определено Четвертым универсальным определением инфаркта миокарда, при исключении обструктивной ишемической болезни сердца (ИБС) [4]. Несмотря на растущее признание, MINOCA остается недодиагностированным и часто неправильно классифицируется из-за сложностей, связанных с определением его основных причин. Стандартная ангиография не всегда выявляет причину ишемии, особенно при диффузном поражении сосудов без обструкции [5].
Причина выделения MINOCA в качестве отдельной нозологической единицы основана на фундаментальных клинических наблюдениях и принципах, таких как: 1) пациенты с MINOCA имеют другой прогноз, чем пациенты с обструктивным поражением; 2) MINOCA может быть вызвана различными атеросклеротическими и неатеросклеротическими причинами с различными патофизиологическими механизмами; и 3) в отличие от ИМ с обструктивным поражением, существует очень мало специализированных исследований, изучающих MINOCA, что приводит к отсутствию основанной на доказательствах терапии у этих лиц [6]. MINOCA характеризуется не только отсутствием выраженной обструкции коронарных артерий, но и разнообразием тканевых повреждений миокарда [7]. Таким образом, MINOCA представляет собой отдельную клиническую единицу, характеризующуюся разнообразными механизмами развития и прогностическими результатами. Несмотря на отсутствие значительной обструкции коронарных артерий, пациенты с MINOCA подвержены риску существенного повреждения сердца и серьезных сердечно-сосудистых событий. В этой связи точная диагностика имеет большое значение в ведении такой группы пациентов.
Цель исследования — изучить тканевые изменения миокарда у пациентов с MINOCA используя магнитно-резонансную томографию.
Материал и методы. В проспективном исследовании приняли участие 94 пациентов с ИМбпST c необструктивным поражением коронарных артерий (MINOCA). Все пациенты выразили информированное согласие на участие в исследовании, и исследование было одобрено экспертным советом. Инфаркт миокарда без подъема сегмента ST определялся в соответствии с Четвертым универсальным определением инфаркта миокарда (2018) [8]. Критерии исключения: значительная ИБС (стеноз ≥ 50%); наличие тромбоэмболия легочной артерии, сепсис, ушиб миокарда; неишемическое повреждение миокарда (миокардит, синдром Такоцубо и кардиомиопатии; пациенты с предшествующим ИМ, предшествующим аортокоронарным шунтированием (АКШ), гемодинамической нестабильностью, необходимостью срочной коронарной реваскуляризации, пациенты со скоростью клубочковой фильтрацией СКФ<30 мл/мин/1,73м2, противопоказаниями к коронарной ангиографии (КАГ) и/или МРТ сердца. Контрольную группу составили 25 человек без сердечно-сосудистых заболеваний. У всех пациентов, включенных в исследование, был собран подробный анамнез, проведен физикальный осмотр и проведена последовательная оценка уровня тропонина с помощью тест-системы ТNT-HS Roche Diagnostics (Германия) с использованием анализатора Cobas 6000 (е 601, Roche, Швейцария). Диапазон измерения этой системы составляет от 0,1 до 2,0 нг/мл. У всех пациентов при поступлении проводился расчёт риска по шкале GRACE (Global Registry of Acute Coronary Events - Глобальный регистр острых коронарных событий). Для оценки тяжести сердечной недостаточности использовали классификацию по Киллипу.
Все пациенты прошли клиническое обследование и стандартную ЭКГ в 12 отведениях. Оценивались изменения сегмента ST, зубца T, наличие патологического зубца Q, а также нарушения ритма и проводимости. Коронарную ангиографию проводили с использованием ангиографической системы Optima IGS 330 (GE, Китай). Значимое поражение коронарных артерий по данным КАГ определялось как сужение просвета более чем на 50% как минимум одной крупной эпикардиальной артерии. Всем пациентам проведена эхокардиография (ЭхоКГ) на аппарате SonoAce R7 (Samsung Medison, Корея) по стандартной методике. МРТ сердца с отслеживанием проводилась на сканерe 3,0 Тл (Philips Achieva). Визуализация с отсроченным усилением выполнялись с использованием стандартных протоколов [9]. Проводился анализ сегментов и количественная оценка объема ИМ и отека. Разделение сегментации левого желудочка и соответствующего кровоснабжения основывалось на сегментах AHA 17 (American Heart Association) [8]. Область кровоснабжения была разделена на область кровоснабжения левой передней нисходящей артерии (LDA), область кровоснабжения левой огибающей артерии (LCX) и область кровоснабжения правой коронарной артерии (RCA). Трансмуральная степень оценивалась с использованием модели AHA для изображений LGE (позднее усиление гадолиния) следующим образом: степень 0, 0%; степень I, 1–25%; степень II, 26–50%; степень III, 51–75%; и степень IV, 76–100% [10]. Для пациентов с MINOCA с несколькими сегментами инфаркта сегмент с самой высокой степенью трансмуральности использовался в качестве степени трансмуральности пациента. Регионарные нарушения движения стенки желудочка оценивались рентгенологами. Аномальные движения стенки желудочка включали уменьшение движения, потерю движения, усиление движения и обратное движение, за исключением диссинхронии. Если в каком-либо одном сегменте миокарда наблюдались аномалии движения стенки, случай отмечался как положительный на аномальное движение стенки.
Размер инфаркта и отека рассчитывали с помощью программного обеспечения Circle Cardiovascular Imaging 42, версия 5.1 (CVI42 V5.1). Площадь инфаркта определяли, как гиперконтрастный миокард на LGE. Размер инфаркта рассчитывали на LGE-изображениях по короткой оси с использованием метода полной ширины на половине максимума и выражали в процентах от общей массы ЛЖ [11]. Площадь отека определяли, как гиперинтенсивную область на T2-STIR-изображениях. Размер отека рассчитывали на T2-STIR-изображениях по короткой оси с использованием автоматизированного метода Оцу и выражали в процентах от общей массы ЛЖ [12].
Статистический анализ выполнен с помощью программы Statistica 10 (StatSoft, США). Статистический анализ полученных результатов включал среднее значение, стандартное и среднее отклонение, минимальные и максимальные значения. Данные были выражены целыми числами и в процентах. Для сравнения данных между группами использовался t-критерий и критерий χ2 с поправкой Йейтса. Значимым считалось р≤0,05.
Результаты. Средний возраст пациентов составил 62,35±10,33 лет (от 33 до 86 лет), мужчины составили 78,7% (n=74), женщины – 21,3% (n=20). В распределении пациентов по возрасту между мужчинами и женщинами статистически значимых различий не выявлено (р> 0,05). При ЭКГ выявлены следующие изменения: депрессия сегмента ST у 57 (60,6%), инверсия зубца T – у 46 (48,9%), у 11 (11,7%) пациентов выявлены нарушения проводимости. Депрессия сегмента ST определялась преимущественно в отведениях V4–V6. Патологический зубец Q отсутствовал во всех случаях. Нарушения проводимости чаще всего, выражалось замедлением внутрижелудочковой проводимости. Частота сердечного ритма варьировала от 68 до 104 уд./мин, в среднем, 83±9 уд./мин. У большинства пациентов – 77 (81,9%) клиническое состояние при поступлении расценивалось как удовлетворительное. Однако у 17 пациентов (18.1%) наблюдались признаки левожелудочковой недостаточности (II класс по Killip). У всех пациентов при поступлении проводился расчёт риска по шкале GRACE, среднее значение которой составило 130±20 баллов, что соответствует умеренному риску неблагоприятных исходов. При анализе традиционных параметров функции сердца не было выявлено значимых различий в фракции выброса (ФВ), конечно-диастолическом объеме левого желудочка (КДОЛЖ), конечно-систолическом объеме левого желудочка (КСОЛЖ), ударном объеме (УО), сердечном выбросе (СВ) и массе миокарда левого желудочка с контрольной группой (таблица 2).
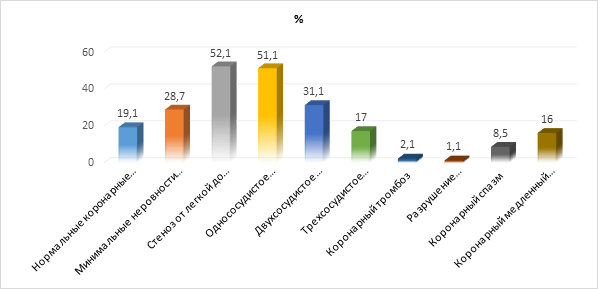
Анализ параметров деформации миокарда, таких как глобальная продольная деформация (GLS), глобальная скорость продольной деформации (GLSR) и глобальная циркулярная деформация (GCS), показал достоверное снижение в группе MINOCA по сравнению с контрольной группой (P < 0,05). Снижение глобальной продольной деформации наблюдалось у пациентов, которые соответствовали диагностическим критериям MINOCA ESC 2018, но имели нормальные результаты традиционной МРТ. Установлено, что у 18 пациентов (19,1%) коронарные артерии были полностью нормальными. У 27 пациентов (28,7%) фиксировались минимальные неровности просвета, что расценивается как ранние или малозначимые структурные изменения без выраженного стенозирования. Наиболее многочисленной оказалась группа пациентов со стенозами лёгкой или умеренной степени — 52,1% (n=49), что подчёркивает гетерогенность морфологических находок у больных с MINOCA. Однососудистое поражение диагностировано у 48 пациентов (51,1%), двухсосудистое — у 30 пациентов (31,9%), а трёхсосудистое — у 16 пациентов (17,0%), что указывает на значительную вариабельность ангиографической картины и потенциальную роль субклинического атеросклероза в патогенезе MINOCA. Коронарный тромбоз выявлен у 2 пациентов (2,1%), признаки разрушения атеросклеротической бляшки — у одного пациента (1,1%). Достаточно часто регистрировались функциональные нарушения: коронарный спазм у 8 пациентов (8,5%) и феномен коронарного медленного кровотока — у 15 пациентов (16,0%). Эти данные подчёркивают мультифакторный характер MINOCA и важность оценки не только анатомических, но и функциональных параметров коронарного кровотока. По результатам МРТ у 94 пациентов с MINOCA было проанализировано 1508 сегментов миокарда, среди которых выявлено 390 сегментов отёка и 255 сегментов инфаркта. Неишемического (субэпикардиального или срединного) отёка или зон позднего контрастирования не выявлено (таблица 3).Большинство инфарктов были малой степени трансмуральности, что типично для MINOCA, где поражения часто ограничены и не охватывают всю толщину миокарда.Неишемические паттерны поражения, включая субэпикардиальный или срединный отёк и зоны позднего контрастирования, не наблюдались, что подтверждает преимущественно ишемическую природу повреждений. Наибольшая частота как отёчных, так и инфарктных изменений регистрировалась в бассейне передней нисходящей артерии (LAD) — 54,9% и 53,7% соответственно, тогда как поражения в зонах кровоснабжения LCX и RCA встречались значительно реже. Анализ степени трансмурального повреждения показал, что большинство инфарктных сегментов характеризовались минимальной глубиной поражения: у 65,9% пациентов трансмуральность не превышала 25%. Эти данные свидетельствуют о преимущественно субэндокардиальном характере ишемии при MINOCA и подчёркивают диагностическую значимость МРТ для выявления малых очагов повреждения миокарда.
Обсуждение. Ранее полагали, что MINOCA может быть связана с лучшим прогнозом по сравнению с ИМбпST с обструктивной ишемической болезнью сердца и не требует дальнейшей диагностики и лечения [13]. Однако, современные исследования показали, что долгосрочная (1–2 года) смертность от всех причин у пациентов с MINOCA составила 2,4–4,7%, что не отличается от пациентов с ИМбпST-ИБС [14, 15]. Следовательно, несмотря на отсутствие явной обструкции коронарных артерий, у пациентов с MINOCA риск неблагоприятного прогноза высок. В данном исследовании мы использовали МРТ и выявили статистически значимые различия деформации миокарда между пациентами с MINOCA и контрольной группой. У пациентов с MINOCA наблюдалось снижение GLS, GLSR и GCS, что указывает на снижение способности к продольной и циркулярной деформации. Наши результаты сопоставимы с данными ряда авторов [16-18]. В нашем исследовании GLS левого желудочка контрольной группы составил −19,20±2,06%, что согласуется с многоцентровым исследованием среди здоровых популяций Восточной Азии [19, 20]. В согласительном документе EACVI/ASE/отраслевой целевой группы по стандартизированной визуализации деформации отмечается, что продольная и циркулярная деформации представлены с отрицательными значениями, и это может привести к путанице. Большее отрицательное значение GLS указывает на укорочение миокарда и лучшую функцию; когда GLS становится менее отрицательным, функция миокарда ухудшается. При сравнении значений деформации следует учитывать абсолютное значение числа [21]. Полученные нами результаты подтвердили патологическую гипотезу, вызывающую MINOCA. Было предложено несколько потенциальных причин MINOCA, которые включают некроз миокарда, вызванный коронарными атеросклеротическими факторами (такими как разрыв бляшки, эрозия бляшки, тромбоз in situ, спонтанное расслоение) и некроз миокарда, вызванный некоронарными атеросклеротическими факторами (такими как спазм эпикардиальных коронарных артерий, коронарная микрососудистая дисфункция, дисбаланс снабжения миокарда кислородом и его потребности) [22]. Из-за ограниченной степени коронарного атеросклероза у пациентов с MINOCA, коронарные атеросклеротические факторы могут играть небольшую роль в этиологии MINOCA. Исследования показали, что коронарная микрососудистая дисфункция широко представлена при различных сердечно-сосудистых заболеваниях, что может быть потенциальным механизмом при MINOCA [23, 24].
Заключение. Проведённый анализ показывает, что МРТ позволяет выявить ключевые структурные особенности миокарда, включая выраженность отёка, степень повреждения тканей и характер позднего контрастирования, что существенно дополняет данные коронарной ангиографии и уточняет патогенетические механизмы заболевания. У пациентов с MINOCA изменения носят гетерогенный характер, что указывает на необходимость комплексного подхода к диагностике, где МРТ занимает ключевое место благодаря высокой точности визуализации и способности дифференцировать различные типы повреждения миокарда. Таким образом, МРТ сердца является незаменимым инструментом в оценке морфологических и функциональных особенностей миокарда у пациентов с MINOCA, позволяя не только уточнить диагноз, но и улучшить стратификацию риска, прогнозирование течения заболевания и выбор оптимальной тактики лечения. Использование МРТ в клинической практике способствует более глубокому пониманию механизмов повреждения миокарда и повышению качества медицинской помощи данной категории пациентов.
Figures

Keywords
References
1.Tognola C, Maloberti A, Varrenti M, Mazzone P, Giannattasio C, Guarracini F. Myocardial Infarction with Nonobstructive Coronary Arteries (MINOCA): Current Insights into Pathophysiology, Diagnosis, and Management. Diagnostics. 2025; 15(7):942. doi: 10.3390/diagnostics15070942
2.Kowallick JT, Scholz M, Schuster A, Lotz J. MINOCA – Myokardinfarkt mit nichtobstruktiven Koronararterien [MINOCA-myocardial infarction with nonobstructive coronary arteries]. Radiologie (Heidelb). 2022;62(11):912-919. German. doi: 10.1007/s00117-022-01079-3.
3.Masood I, Hafeez I, Rashid A, Rasool V, Ajaz S, Dar MI, et al. Role of cardiac magnetic resonance imaging in identifying infarct related artery and non-ischemic pathogenesis in patients presenting with non ST elevation myocardial infarction. Indian Heart Journal.2024;76(2):101-107. doi: 10.1016/j.ihj.2024.02.004
4.Сафонова Е.А., Сукманова И.А. Инфаркт миокарда без обструктивного поражения коронарных артерий (MINOCA). Клиническая медицина. 2020;98(2):89–97. DOI doi: 10.30629/0023-2149-2020-98-2-89-97
5.Riahi F, Tooyserkani SH, Mojahedi A, Dormiani-Tabatabaei SA, Fesharaki S, Azizollahi S, et al. Cardiac magnetic resonance imaging in myocardial infarction with non-obstructed coronary arteries: diagnostic and prognostic value. Am J Cardiovasc Dis. 2025 Apr 25;15(2):56-68. doi: 10.62347/FCDC4114.
6.Ezhumalai B, Modi R, Chidambaram S. A comprehensive review on myocardial infarction with non-obstructive coronary arteries (MINOCA): One size does not fit all. Indian Heart Journal. 2025;77(4): 318-325. doi: 10.1016/j.ihj.2025.05.013
7.Daneshrad JA, Ordovas K, Sierra-Galan LM, Hays AG, Mamas MA, Bucciarelli-Ducci C, et al. Role of Cardiac Magnetic Resonance Imaging in the Evaluation of MINOCA. J Clin Med. 2023;12(5):2017. doi: 10.3390/jcm12052017.
8.Thygesen K, Alpert JS, Jaffe AS, Chaitman BR, Bax JJ. Morrow DA, et al. Fourth universal definition of myocardial infarction (2018). Eur Heart J. 2019; ehy462/ 40(3):237-269. doi: 10.1093/eurheartj/ehy462.
9.Kramer CM, Barkhausen J, Bucciarelli-Ducci C, Flamm SD, Kim RJ, Nagel E. Standardized cardiovascular magnetic resonance imaging (CMR) protocols: 2020 update. J Cardiovasc Magn Reson. 2020;22(1):17. doi: 10.1186/s12968-020-00607-1.
10.Milotta G, Munoz C, Kunze KP, Neji R, Figliozzi S, Chiribiri A, et al. 3D whole-heart grey-blood late gadolinium enhancement cardiovascular magnetic resonance imaging. J Cardiovasc Magn Reson. 2021;23(1):62. doi: 10.1186/s12968-021-00751-2.
11.Sjögren J, Ubachs JF, Engblom H, Carlsson M, Arheden H, Heiberg E. Semi-automatic segmentation of myocardium at risk in T2-weighted cardiovascular magnetic resonance. J Cardiovasc Magn Reson. 2012;14(1):10. doi: 10.1186/1532-429X-14-10.
12.Flett AS, Hasleton J, Cook C, Hausenloy D, Quarta G, Ariti C, et al. Evaluation of techniques for the quantification of myocardial scar of differing etiology using cardiac magnetic resonance. JACC Cardiovasc Imaging. 2011;4(2):150-6. doi: 10.1016/j.jcmg.2010.11.015.
13.McCabe JM, Armstrong EJ, Kulkarni A, Hoffmayer KS, Bhave PD, Garg S, et al. Prevalence and factors associated with false-positive ST-segment elevation myocardial infarction diagnoses at primary percutaneous coronary intervention–capable centers: a report from the Activate-SF registry. Arch Intern Med. 2012;172(11):864-71. doi: 10.1001/archinternmed.2012.945.
14.Barr PR, Harrison W, Smyth D, Flynn C, Lee M, Kerr AJ. Myocardial Infarction Without Obstructive Coronary Artery Disease is Not a Benign Condition (ANZACS-QI 10). Heart Lung Circ. 2018 Feb;27(2):165-174. doi: 10.1016/j.hlc.2017.02.023.
15.Pasupathy S, Tavella R, Beltrame JF. Myocardial Infarction With Nonobstructive Coronary Arteries (MINOCA): the past, present, and future management. Circulation. 2017;135:1490–1493. doi: 10.1161/CIRCULATIONAHA.117.027666.
16.Heitner JF, Senthilkumar A, Harrison JK, Klem I, Sketch MH Jr, Ivanov A, et al. Identifying the Infarct-Related Artery in Patients With Non-ST-Segment-Elevation Myocardial Infarction. Circ Cardiovasc Interv. 2019;12(5):e007305. doi: 10.1161/CIRCINT. ERVENTIONS.118.007305.
17.Bhatia S., Anstine C., Jaffe AS, Gersh BJ, Chandrasekaran K., A Foley T., et al. Магнитно-резонансная томография сердца у пациентов с повышенным тропонином и нормальной коронарной ангиографией. Heart. 2019;105:1231–1236. doi: 10.1136/heartjnl-2018-314631.
18.Li, Y., Huang, R., Zheng, S, Huang D, Lin W, Lin G, et al. Myocardial strain analysis by feature tracking cardiac magnetic resonance to identify subclinical cardiac dysfunction in patients with MINOCA. J Cardiothorac.2024;602. doi:. 10.1186/s13019-024-03093-z
19.Asch FM, Miyoshi T, Addetia K, Citro R, Daimon M, Desale S et al. Similarities and differences in left ventricular size and function among races and Nationalities: results of the World Alliance societies of Echocardiography normal values study. J Am Soc Echocardiogr. 2019;32:1396 – 406.e2
20.Li G, Zhang Z, Gao Y, Zhu C, Zhou S, Cao L, et al. Age- and sex-specific reference values of biventricular strain and strain rate derived from a large cohort of healthy Chinese adults: a cardiovascular magnetic resonance feature tracking study. J Cardiovasc Magn Reson. 2022 Nov 21;24(1):63. doi: 10.1186/s12968-022-00881-1.
21.Voigt JU, Pedrizzetti G, Lysyansky P, Marwick TH, Houle H, Baumann R, et al. Definitions for a common standard for 2D speckle tracking echocariography: consensus document of the EACVI/ASE/Industry Task Force to standardize deformation imaging. Eur Heart J Cardiovasc Imaging. 2015;16(1):1-11. doi: 10.1093/ehjci/jeu184.
22.Talebi S, Jadhav P, Tamis-Holland JE. Myocardial Infarction in the Absence of Obstructive Coronary Artery Disease (MINOCA): a Review of the Present and Preview of the Future. Curr Atheroscler Rep. 2021;23(9):49. doi: 10.1007/s11883-021-00945-0.
23.Sucato V, Novo G, Saladino A, Evola S, Galassi AR. Coronary microvascular dysfunction. Minerva Cardioangiol. 2020 Apr;68(2):153-163. doi: 10.23736/S0026-4725.20.05070-7.
24.Padro T, Manfrini O, Bugiardini R, Canty J, Cenko E, De Luca G, et al. ESC Working Group on Coronary Pathophysiology and Microcirculation position paper on 'coronary microvascular dysfunction in cardiovascular disease'. Cardiovasc Res. 2020;116(4):741-755. doi: 10.1093/cvr/cvaa003.
Article Info:
Publication history
Published: 28.Jun.2025
Copyright
© 2013-2025. Azerbaijan Society of Cardiology. Published by "Uptodate in Medicine" health sciences publishing. All rights reserved.Related Articles
Viewed: 558


